Nat. Commun. | 通过调制激发态构象实现对映体识别可视化

今天与大家分享一篇发表在Nat. Commun.上的文章,标题是“通过调制激发态构象实现对映体识别可视化”。本文的通讯作者是华东理工大学的马骧教授。
手性作为分子结构的基本属性,在药物研发和材料科学等众多领域都发挥着关键作用,因此对手性对映体进行识别与分离至关重要。基于发光现象的分析技术已成为替代高效液相色谱的有力方案,其具有操作简便、检测快速以及可实现实时监测等优势。然而,在手性识别过程中,由于系综平均效应的影响,宏观测量的灵敏度往往会降低。尽管科学家们在利用功能性染料开发手性识别技术方面已取得了诸多成果,但目前仍迫切需要简便、快速且灵敏的手性识别产品。该领域的核心挑战在于如何利用染料与对映体之间的差异化相互作用,精确调控染料的发射能级,从而实现对手性对映体的高灵敏度区分。
科研人员最近发现了一类具有振动诱导发光(VIE)效应的荧光团分子。该分子在溶液中会发生激发态构型转变,通过有效的π共轭作用产生红色荧光;而在固态或聚集状态下,由于物理约束,阻碍了激发态结构向平面化发生转变,导致其具有固有蓝光发射。与传统荧光团不同,VIE染料的荧光特性能够随微环境变化而发生动态调控。这种激发态敏感性可放大手性空间中组装的细微变化,使VIE染料特别适用于手性识别。有人曾将VIE体系与石墨烯结合构建单分子器件,通过电导状态下的区分实现了单分子水平的手性识别原位实时观测。然而该方法的仪器检测前样品预处理及后续分析均需在苛刻条件下进行。
作者在这里通过将识别单元2-氨基-1,2-二苯基乙醇引入VIE分子,设计并合成了具有可视化手性识别功能的有机染料。如图1所示,利用染料与手性小分子之间的选择性共组装机制,在一定条件下精确调控了VIE染料的激发态构象。发光颜色的差异使得对映体识别及对映体过量值分析成为可能。此外,通过采用数码摄影和手持光学探测器量化了红-绿-蓝(RGB)色值与CIE色坐标同对映体过量值之间的关联,最终建立了用于分析手性小分子对映体过量值的光学显示系统。本研究致力于将单分子水平的微观动态变化精确放大至肉眼可辨的宏观状态,从而实现实时、高灵敏度、可视化的手性区分。
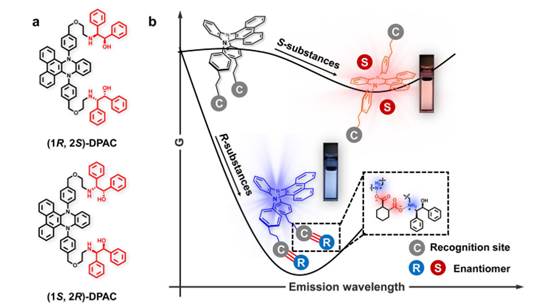
图1、对映体识别结构与表征。a:手性分子(1S,2R)-及(1R,2S)-DPAC的化学结构。b:对映体识别可视化示意图。
作者通过将手性识别助剂(1S,2R)-或(1R,2S)-1,2-二苯基-2-氨基乙醇以烷基链为桥连单元引入VIE染料中,成功制得手性颜色指示剂。采用核磁共振氢谱、碳谱及电喷雾电离高分辨质谱分析确认了其分子结构。1,2-二苯基-2-氨基乙醇结构单元在手性识别过程中起驱动作用,这归因于其对映体特异性“定向附着”作用与手性分子之间产生的空间匹配,其精确的取向与空间排列使其能够形成特定的非共价相互作用。图2b的荧光光谱所示,(1S,2R)-DPAC表现出典型的振动诱导发光特性:在固态与溶液中呈现差异化荧光发射,表明手性识别助剂的引入不会影响VIE染料激发态构型的转变。
随后作者通过分析测试量化了(1S,2R)-DPAC对手性底物的立体选择性结合能力。如图2c的荧光光谱所示,新制备的(1S,2R)-DPAC溶液在600 nm处呈现强红色发射。加入(1R,2R)-环己烷-1,2-二羧酸(R-1)后,600 nm处荧光强度显著降低,同时在460 nm处出现新的发射带。样品发生了显著的颜色变化——从初始红色转变为明显蓝色,当加入2.0当量R-1后,光致发光不再产生可观测到的变化。相比之下,加入立体异构构型相反的(1S,2S)-环己烷-1,2-二羧酸(S-1)时,体系产生的发光扰动显著减弱(图2d)。基于VIE染料的双发射特性,比率荧光(I460 nm/I600 nm)在不同构型手性化合物滴定过程中表现出了显著变化。作者进一步通过优化浓度与溶剂比例进行了相关研究。在测得的最佳条件下,光学照片与CIE色度图分析表明:引入不同对映体时发光特性呈现显著差异(图2e,f)。该过程的高量子产率使得无需进行繁琐的多步操作即可实现手性的可视化区分,这种简化的方法显著提升了手性检测的效率与适用性。
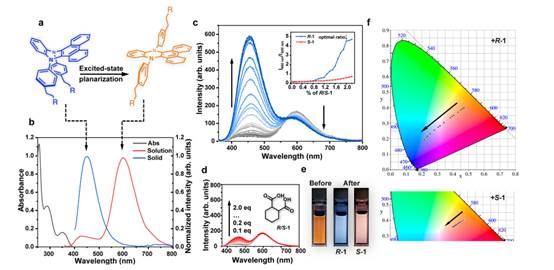
图2、对映体识别的光学特性。a:VIE机制示意图。b:(1S,2R)-DPAC在丙酮中的吸收光谱与荧光光谱(浓度=1.0×10⁻⁵ M,激发波长λex=350 nm)。c,d:(1S,2R)-DPAC与不同比例(0.00-2.00当量)R-1及S-1混合后的荧光光谱,插图为比率荧光强度变化。e:(1S,2R)-DPAC与R/S-1混合前后的光学照片。f:不同比例混合样品的1931 CIE色度坐标图(溶剂:环己烷/丙酮=5:1,浓度=1.0×10⁻⁴ M,λex=350 nm)。
基于上述现象,作者进一步考察了其他常见芳香族手性化合物及氨基酸。(1S,2R)-DPAC在环己烷/丙酮(5/1, v/v)体系中持续展现出卓越的可视化手性区分能力:当加入2.0当量不同构型的手性化合物时,体系均呈现显著的发光差异。利用这一特性,仅通过简单目视检测即可快速识别手性化合物构型,该方法适用于氨基酸及其衍生物、手性酸以及扁桃酸等药物分子,展现出广泛的普适性(详见表1)。鉴于1,2-二苯基-2-氨基乙醇单元具有两个手性中心的结构特性,其并非仅对R型对映体呈现高结合亲和力。相反,在某些情况下该体系对S型对映体也表现出了较强的结合能力。但不同构型分子间差异化的亲和力,始终能够有效促进对映选择性识别能力的实现。
随后作者研究了可视化识别的机制。基于VIE原理,观测到的显著光致发光变化可归因于不同分子聚集态的形成。在这些组装体中,振动诱导的激发态平面化过程被显著抑制,从而产生固有的蓝色荧光发射。作者采用了动态光散射(DLS)技术研究了自组装过程:在该混合溶剂体系中,手性分子的引入导致(1S,2R)-DPAC体系产生显著的粒径变化,证实了差异化组装体的形成(图3a)。此外,组装体的刚性化效应有效抑制了荧光非辐射跃迁,使460 nm和600 nm处的发光寿命均显著增强(图3c)。
对映体选择性的主要决定因素来源于焓变差异,且焓熵补偿效应同样被证实是调控对映体选择性的关键因素。(1S,2R)-DPAC分子结构中的氨基作为有效的质子受体,易在酸性环境中形成离子复合物。作者推测所形成的离子化合物溶解度降低,这是诱导聚集体形成并改变VIE分子激发态构象的关键因素。为验证这一猜想,作者采用盐酸滴定促使离子化合物产生沉淀:如图3b所示,随着不同摩尔比盐酸的加入,(1S,2R)-DPAC呈现出类似的发光变化趋势。本研究还选取了两个参照化合物:缺乏质子供给能力的R-Dic和具有强碱性的D-Glu。实验结果表明这两种化合物均无法诱导(1S,2R)-DPAC形成(-NH2+-)结构,因而不能引起发光颜色变化(图3d)。由此可见,(1S,2R)-DPAC与手性酸分子的组装过程通过氢键相互作用实现,该作用机制是光致发光特性调控的驱动力。
为深入探究对映体选择性识别过程的作用机制,作者采用1H-NMR滴定以确定(1S,2R)-DPAC与手性分子的具体结合位点。由于(1S,2R)-DPAC与R-1在(CD3)2CO中混合后因溶解度降低形成分子聚集体沉淀,阻碍了分子间相互作用信号的检测,故选择CDCl3作为溶剂。如图3e所示,(1S,2R)-DPAC与R-1的组装导致两组分质子共振均发生显著扰动,所形成的氨基阳离子(-NH2+-)具有显著降低邻近质子电子密度的能力,从而引起NMR谱图向低场发生位移。这些结果证明了-NH2+-结构的形成是发光特性改变的关键因素,也是实现可视化进行手性辨别的基础。
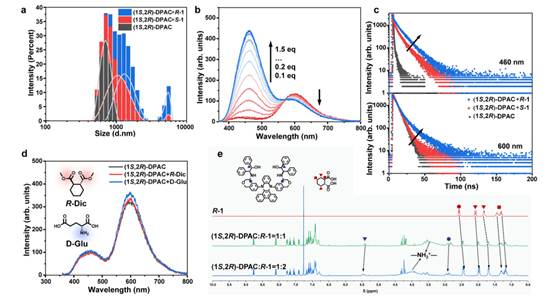
图3、可视化识别机制。a:(1S,2R)-DPAC与R/S-1混合后的动态光散射(DLS)分析。b:(1S,2R)-DPAC与不同比例HCl混合后的荧光光谱。c: (1S,2R)-DPAC与R/S-1混合后的发光衰减寿命。d:(1S,2R)-DPAC与R-Dic及D-Glu混合后的荧光光谱。实验条件:[(1S,2R)-DPAC]=1.0×10⁻⁴ M(环己烷/丙酮=5:1),[(1S,2R)-DPAC]/[对映体]=1/2,λex=350nm。e:(1S,2R)-DPAC与R-1在CDCl3中混合后的¹H-NMR谱图(400MHz, 298K)。
圆偏振发光(CPL)可反映手性发光体系的激发态结构信息。加入对映体后,(1S,2R)-DPAC的CPL信号变化趋势与其荧光光谱高度一致。圆二色性(CD)与CPL光谱方向的一致性表明:手性小分子的相互作用未改变(1S,2R)-DPAC的手性光学构型(图4a)。在确定构型未发生反转的基础上,作者采用基于B3LYP/6-311g*模型进行几何优化确定了分子最低能量态的原子构型。计算结果显示:(1S,2R)-DPAC与R/S-1混合后更倾向于以U型堆叠模式存在,该构型具有较低势能(图4c)。基于此最优结构,采用M06-2X/DEF2-TZVP方法组计算了(1S,2R)-DPAC与R/S-1对映体的相互作用能。经基组重叠误差校正后,其与R型和S型对映体的相互作用能分别为-22.49 kcal/mol和-19.49 kcal/mol。此外,通过等温滴定微量热(ITC)实验评估了(1S,2R)-DPAC与R/S-1的结合行为,ITC数据明确揭示了对映体间结合常数的差异(图4b)。
此外,通过形貌表征也观察到了相互作用的差异性。(1S,2R)-DPAC与不同构型R/S-1的相互作用导致颗粒数量产生显著差异。具体而言:与R-1化合物作用后形成的组装体不仅粒径增大,其数量也会增加。当手性酸的对映体具有与(1S,2R)-DPAC相匹配的立体化学构型时,会因溶解度降低而形成聚集体。这种聚集作用抑制了振动诱导的(1S,2R)-DPAC激发态平面化过程,最终导致蓝光发射(图4d)。
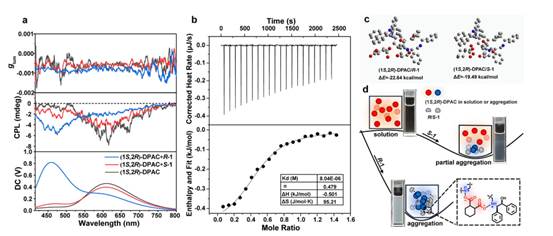
图4、对映选择性相互作用与几何优化。a:(1S,2R)-DPAC与R/S-1混合后的圆偏振发光(CPL)谱。实验条件:[(1S,2R)-DPAC]=1.0×10⁻⁴ M(环己烷/丙酮=5:1),[(1S,2R)-DPAC]/[对映体]=1/2,λex = 350 nm。b:(1S,2R)-DPAC与R-1在丙酮中的等温滴定微量热(ITC)数据。样品池:[(1S,2R)-DPAC]=100 μM,[注射器:R-1]=1 mM,298K。c:基于B3LYP/6-311g*方法和M06-2X/DEF2-TZVP基组计算的(1S,2R)-DPAC与R/S-1对映体的相互作用能及优化结构。d:对映体识别可视化机制示意图。
对映体酸与(1S,2R)-DPAC的立体选择性组装赋予了超分子复合物可调控的发光特性。波长差异产生的发光区分使对映体鉴别更加高效,这为开发高保真、高灵敏度的分析技术以量化手性小分子对映体过量值(ee%)提供了新途径。以R/S-1为例:当(1S,2R)-DPAC与手性分子的摩尔比保持在1:2时,随着对映体过量值从+100%到-100%的全范围变化,体系比率荧光强度(I460 nm/I600 nm)呈现系统性衰减(图5a)。相反,(1R,2S)-DPAC则表现出近乎完美的镜像对称性。比率荧光强度与对映体过量值之间存在显著的非线性关系,通过曲线拟合可建立校准曲线,可用于测定未知样品的对映体组成,从而实现基于荧光光谱变化的ee%定量检测。进一步建立比率荧光强度与ee%的关联模型后,可有效规避测试条件对检测信号的影响。在不同测试条件下对多组未知样品进行测定,测得ee值与实际值的平均绝对误差(AAE)为2.55% ee。
不同ee%值下的发光颜色差异可通过CIE色度图与光学图像清晰辨识(图5b)。这种显著的发光颜色变化使得仅通过视觉观察即可初步判定ee%值,为开发可视化ee%比色传感器提供了建设性策略。作者系统采集了不同ee%值样品的发光照片,但考虑到不同成像设备感光元件的固有差异及环境光照对拍摄结果的影响,在这里采用了标准色卡对样品真实发光状态进行了校正。
通过数码摄影技术将未知样品转换为RGB色值(图5c,d),但RGB值的变化仅在特定ee%范围内呈现线性关系,可能略微影响实际应用。随后作者使用了可直接获取样品光学数据(如CIE坐标)的手持光学检测仪,绘制出CIE坐标与ee%的关联曲线,展现出显著线性相关性,大幅提升了检测灵敏度与便捷性(图5d)。由此无需光谱仪器,仅通过分析RGB通道亮度分布或CIE坐标即可推导样品ee%(图5e)。该策略的简易性在手性试剂鉴定领域展现出重要应用潜力。
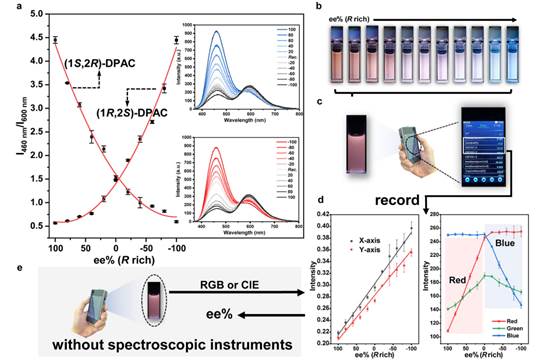
图5、对映体过量分析的光学特性。a:(1S,2R)-或(1R,2S)-DPAC与不同对映体含量的R/S-1混合后460 nm/600 nm相对荧光强度变化。插图:不同对映体含量混合后样品的荧光光谱。b:不同对映体含量混合后样品的光学照片。c:手持光学测试仪记录CIE坐标示意图。d:CIE坐标及RGB值随R/S-1对映体过量值(ee%)的变化曲线(误差棒数据表示为均值±标准差,n=3个独立样品)。e:对映体过量分析示意图。实验条件:[(1S,2R)-或(1R,2S)-DPAC]=1.0×10⁻⁴ M(环己烷/丙酮=5:1),[(1S,2R)-或(1R,2S)-DPAC]/[R/S-1]=1/2,λex=350 nm。
综上所述,本研究通过将识别单元2-氨基-1,2-二苯基乙醇引入振动诱导发光分子,成功设计并合成了具有可视化手性识别功能的分子探针。利用非共价相互作用驱动染料与手性小分子之间的选择性组装,精确调控了VIE染料的激发态构象。这种精准操纵实现了多种手性化合物的可视化区分。此外,发光颜色的差异使得对映体识别及对映体过量值分析成为可能。通过将光学信号进一步转换为RGB色值与CIE坐标并进行定量分析,建立了用于手性小分子对映体过量值分析的光学显示系统。该策略为对映选择性识别和对映体过量值分析提供了一种简便高效的方法。
文字:张玺
审核:叶曦翀
参考文献:DOI: 10.1038/s41467-025-63065-2
https://doi.org/10.1038/s41467-025-63065-2