Chinese Chemical Letters |水中手性氨基酸识别:一种基于BINOL的荧光探针
今天与大家分享一篇发表在Chinese Chemical Letters上的文章,标题是“水中手性氨基酸识别:一种基于BINOL的荧光探针”。本文的通讯作者为武汉工程大学的古双喜教授。
手性氨基酸在生命系统中发挥着重要而多样的作用,是多种功能性有机分子的重要合成子和手性来源。因此,氨基酸的手性分析近年来备受关注。荧光探针作为识别手性分子的方法之一,具有分析速度快和可对手性底物进行直接成像等优点。一些实验室已经开始对游离氨基酸的手性荧光识别进行研究。2014年,蒲林教授和余孝其教授课题组合作报道了1,1’-联二萘酚(BINOL)基化合物(S)-1(图1)在Zn(II)存在下作为手性荧光探针,用于对包括游离氨基酸在内的手性胺类化合物具有较优秀的识别能力。2019年,作者团队报道了一种荧光探针(S,S)-2(图1) 对各种游离氨基酸具有高对映选择性,在CH3CN/H2O混合溶剂中Zn(II)存在下,可用于确定氨基酸的对映体组成。然而,由于水溶性较差的原因,该荧光探针不能在只有一种溶剂水的条件下进行手性氨基酸识别。
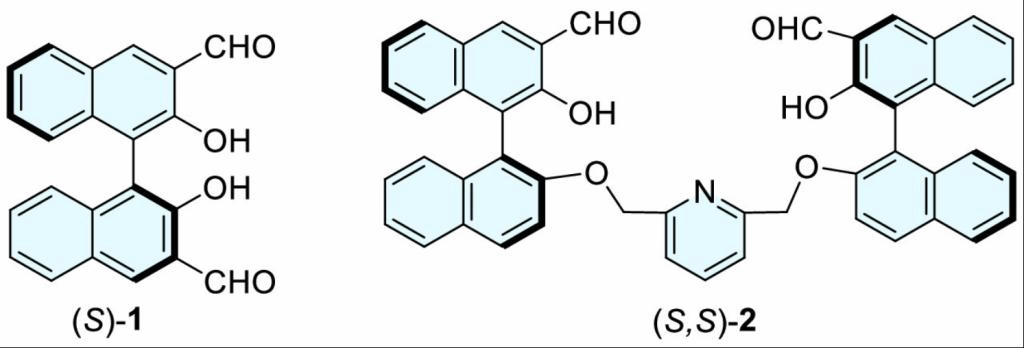
图1 (S)-1和(S,S)-2的结构
而水溶性荧光探针的发展具有重要意义。一方面,由于大多数氨基酸具有优异的水溶性,有利于扩大氨基酸手性识别的应用范围。另一方面,它可以有效地消除荧光检测中不溶水的杂质的干扰。为了提高BINOL基手性荧光探针的水溶性,作者团队提出了以下三种策略。第一种,将各种亲水性侧链通过铃木偶联反应连接在(S)-1的6,6’位置,得到(S)-3(图2)。第二种,在水中使用亲水性胶束封装(S)-1。第三种,通过在(S)-1的3,3’位置(如(R,R)-4(图2))安装咪唑,或在6,6’位置入磺酸盐片段 (如(R)-5(图2))将探针修改为水溶性盐。其中,第三种策略以其简洁的合成方法和对水溶性的极大改善而更具价值。
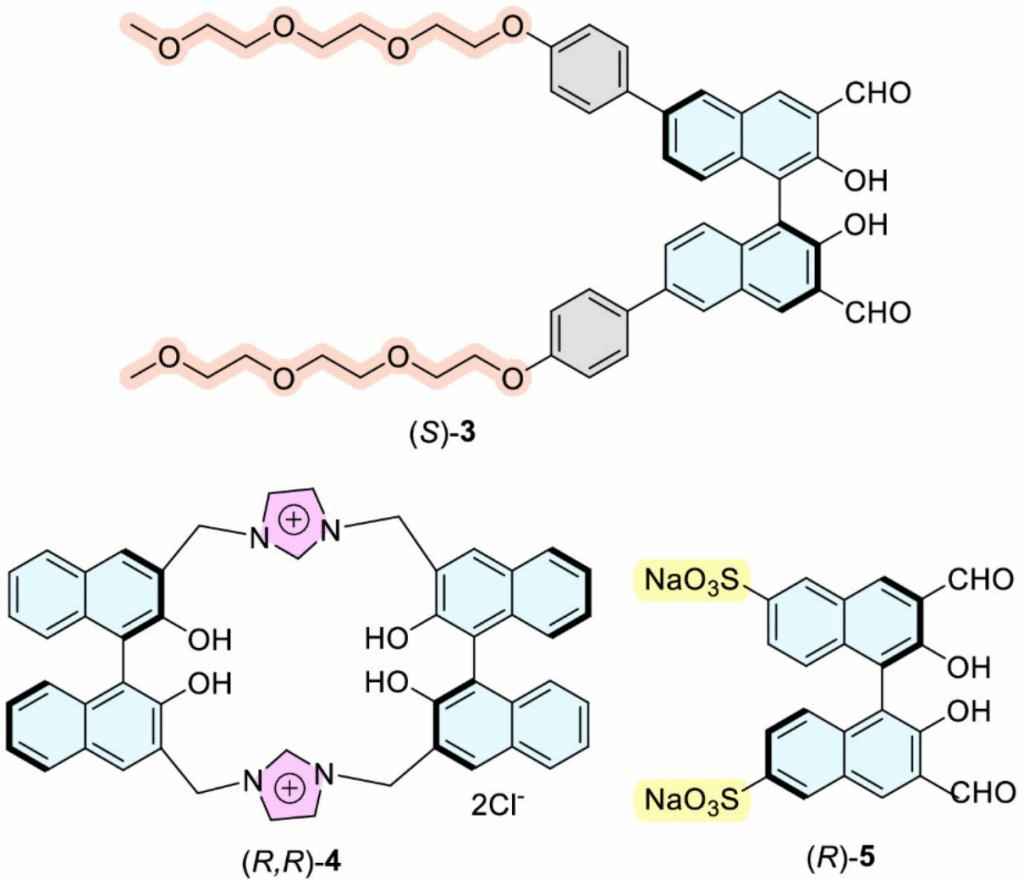
图2 具有代表性的水溶性荧光探针的结构
此外,在BINOL基荧光探针手性识别氨基酸的研究中,快速的荧光响应和持续的稳定性一直是研究者追求的目标。然而,目前报道的BINOL基探针对手性氨基酸的荧光响应通常至少在2~3 h后才能达到稳定,有些探针甚至需要在低温或其他方式下进行猝灭才能进行荧光检测。
在本研究中作者设计了一种新型荧光探针(S)-6(图3),其2’位置有一个磺酸钠片段可以与Zn(II)形成配合物,提高稳定性。进行氨基酸手性识别的可能的作用模式如图3所示。在室温下探针(S)-6对氨基酸的荧光响应仅需30 min即可达到最大值且稳定时间至少为5.5 h,不但节省了时间且有利于手性荧光分析的可操作性和可重复性。
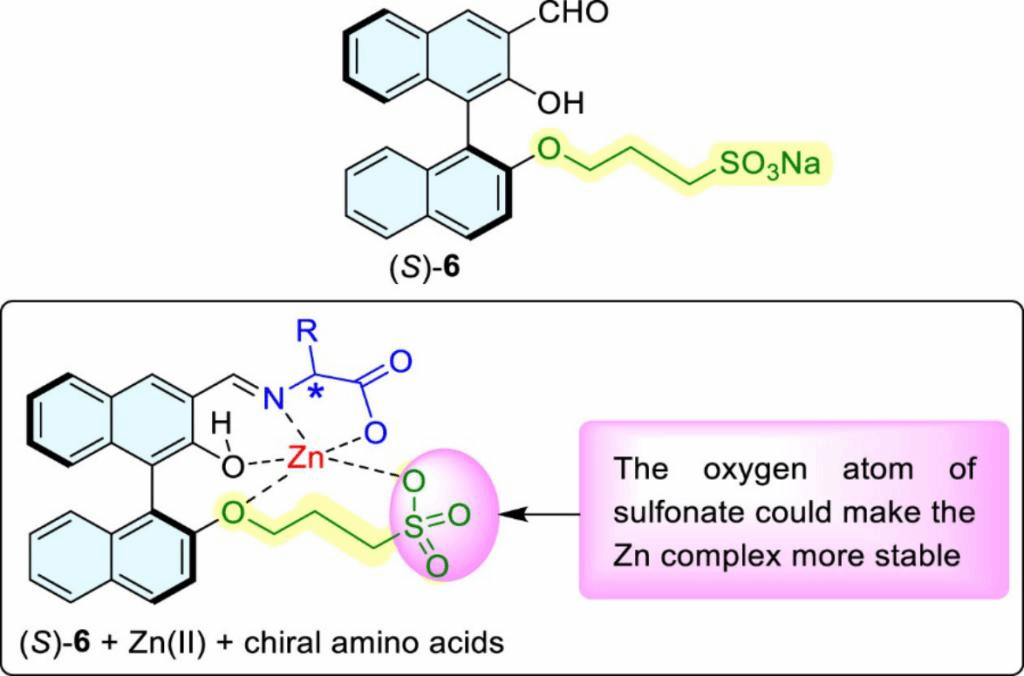
图3 (S)-6的结构和其进行氨基酸手性别可能的作用模式
方案1是合成荧光探针(S)-6的一种简洁高效的方法。以1,3-丙磺酸内酯为磺化剂,将原料(S)-7磺化得到中间体(S)-8,比之前文献中所报道的以浓硫酸为原料的磺化方法更温和,原子利用率更高。然后在HCl/H2O/CHCl3存在下脱去 (S)-8中起保护作用的甲氧基(MOM)基团,再加入NaHCO3至溶液pH呈碱性,得到目标探针(S)-6。
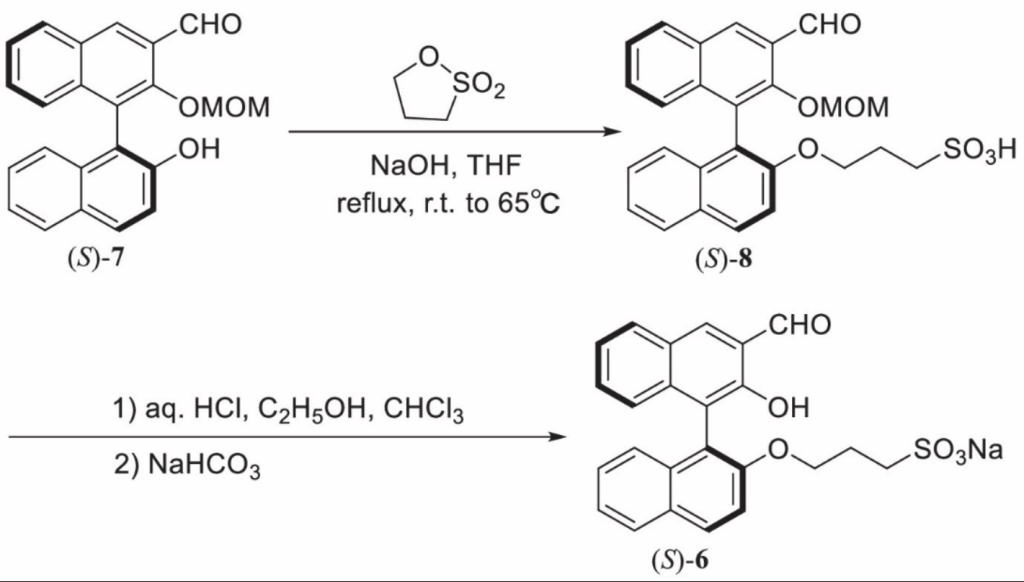
方案1 (S)-6的合成路线
合成的探针(S)-6具有良好的水溶性。(S)-6的水溶液在加入或不加入Zn(II)时均无荧光反应。然而,加入L-色氨酸或D-色氨酸后,在Zn(II)存在下,溶液在539 nm处对映选择性荧光增强(图4a)。
Zn(II)对探针对氨基酸的对映选择性识别的影响如图4b所示,在Zn(OAc)2 和(S)-6摩尔比从0:1变化到20:1范围内,含L-Trp或D-Trp的探针溶液在539 nm处的荧光强度随着Zn(II)的增加而明显增强且含L-Trp的溶液比含D-Trp的溶液的增强幅度更大。结果表明,与Zn(II)的络合有利于提高探针(S)-6对氨基酸的对映选择性。已知荧光在高浓度下具有自猝灭现象,所以荧光测量通常在微摩尔或纳摩尔浓度下进行。但在高浓度下荧光探针和手性底物之间才有良好的反应性。探针(S)-6在微摩尔浓度下对色氨酸仍表现出良好的反应性,适合于荧光测试。在图4(b)中,作者比较了两种不同浓度的结果,结果表明,两种方法的荧光响应非常相似而高浓度更有效。
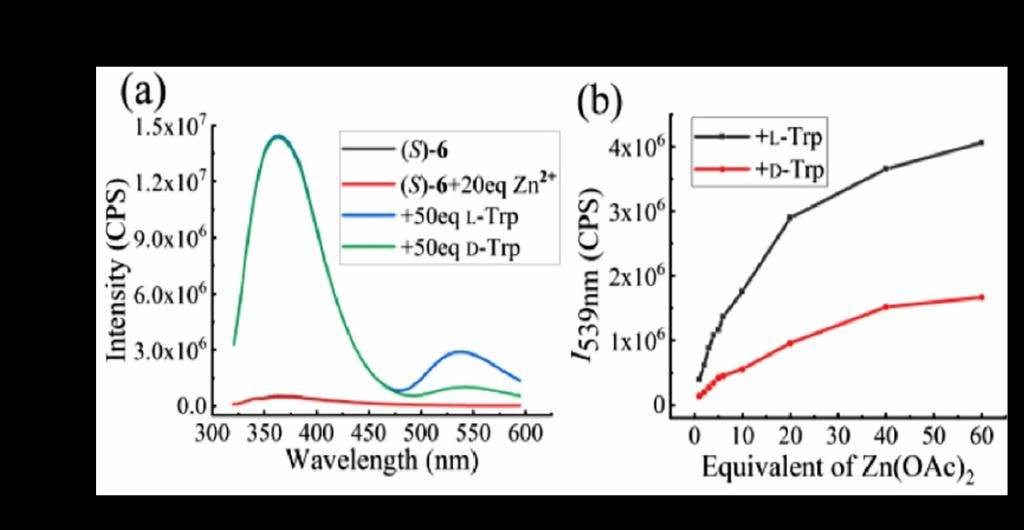
图4 (a) D-和L -色氨酸在Zn(OAc)2 :(S)-6 = 20:1的荧光光谱;(b)在539 nm处对D-和L-色氨酸的荧光强度与等效Zn(OAc)2的对比。上述混合物先在0.2 mmol/L (S)-6的条件下静置2 h,(b)然后稀释至33 mmol/L后进行荧光检测。
此外,研究了Zn(OAc)2 和(S)-6摩尔比为20:1的浓度低至 33 mmol/L的水溶液中 (S)-6的荧光稳定性。如图5所示,在539 nm处监测了混合时间为0~6 h的荧光强度,在最初的30 min内 (S)-6对L-色氨酸和D-色氨酸有明显荧光增强并在30 min处达到最大值,接下来的5.5小时往往可以保持稳定。该探针更快的荧光响应速度和更好的稳定性有利于提高手性氨基酸识别的时效性和可重复性。
以(R)-7为原料,仍按照方案1的路线制备(S)-6的对映体(R)-6。在相同的条件下研究(R)-6对D-和L-Trp的荧光响应。如图6所示,与(S)-6 + Zn(II)的组合对手性色氨酸的荧光光谱一样,加入色氨酸对映体后,539 nm处的荧光强度呈现对映选择性增强,但对L-色氨酸和D-色氨酸的相对强度刚好相反。通过对比图6和图4a,可以发现(R)-6和(S)-6对D-和L-色氨酸的荧光响应曲线呈镜像关系,证实了荧光探针对手性色氨酸的对映选择性识别作用。
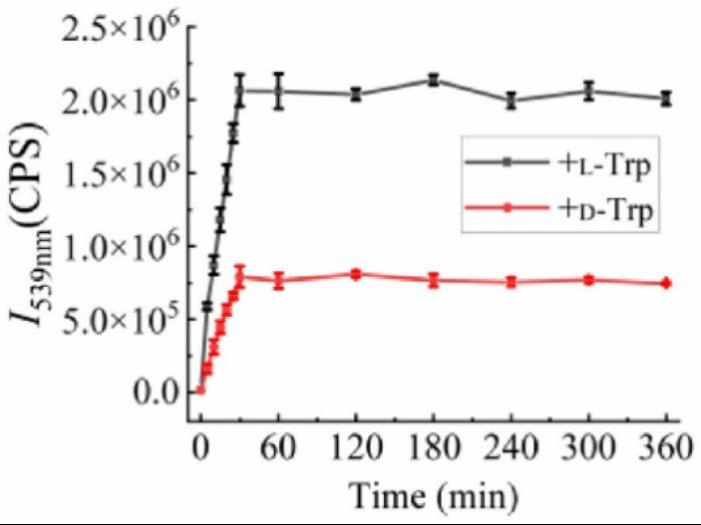
图5 539 nm处,混合时间为0 ~ 6 h,Zn(OAc)2 和(S)-6摩尔比为20:1的浓度低至 33 mmol/L的水溶液中 (S)-6对L-和D-色氨酸的荧光稳定性。

图6 D-和L -色氨酸在Zn(OAc)2 :(R)-6 = 20:1的荧光光谱。
此外,作者还考察了(S)-6对其他18种常见氨基酸的荧光响应。在与色氨酸相同的条件下,除脯氨酸、天冬氨酸和半胱氨酸外,其余15种氨基酸如精氨酸、丝氨酸、缬氨酸、天冬氨酸、赖氨酸、苯丙氨酸、谷氨酰胺、亮氨酸、蛋氨酸、组氨酸、苏氨酸、丙氨酸、谷氨酰胺、酪氨酸和异亮氨酸均有明显的对映选择性增强。(S)-6、(S)-6 + Zn(II)、(S)-6 + Zn(II) + L-/D-氨基酸在550 nm处的相对荧光强度如图7所示。对于上述15种氨基酸,(S)-6对L-对映体的荧光强度均强于对应的D-对映体。表明该探针对水溶液中氨基酸的对映选择性识别具有普适性,可广泛用于各种氨基酸的手性识别。
浓度和光学纯度是手性物质的两个重要参数。因此,作者团队探讨了这两个因素与探针荧光强度的依赖关系。分别用色氨酸与(S)-6的摩尔比值和D-色氨酸的对映体过量值(ee/% = [D−L]/[D + L])描述浓度和光学纯度。图8显示了色氨酸摩尔比分别在360 nm和539 nm处与荧光强度的关系。
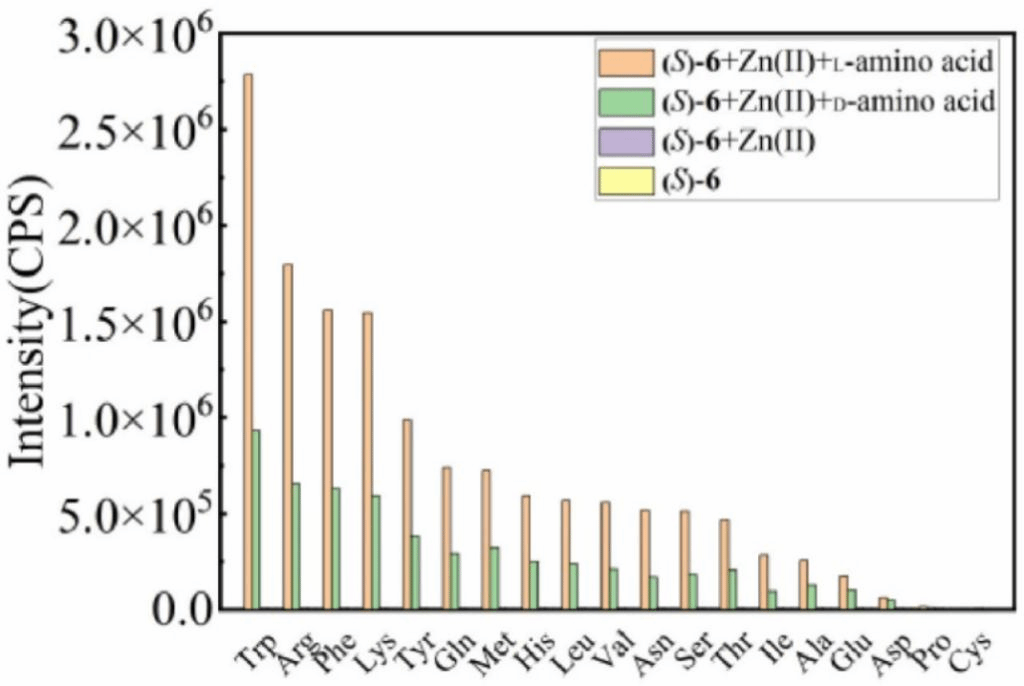
图7 (S)-6 + Zn2+(1:20)与19对D-/L-氨基酸(包括色氨酸)的混合物在550 nm处的荧光响应。
360 nm处的荧光发射峰归属于色氨酸。色氨酸的量在0~20 mol范围内,360 nm处荧光强度与色氨酸浓度之间保持线性关系,不受探针与Zn(II)相互作用的干扰。539 nm处的荧光发射峰在所研究的色氨酸含量范围内显示出了对映选择性增强。
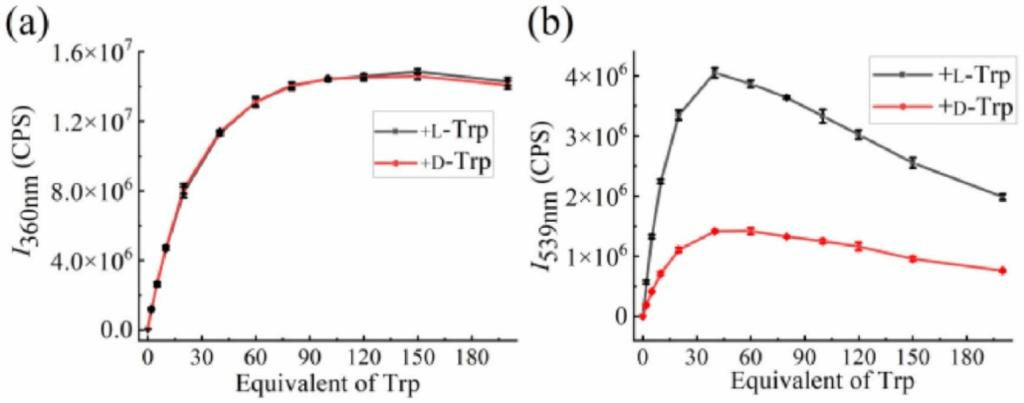
图8 (a)360nm (I360nm)和(b) 539nm (I539nm)与D-和L-色氨酸等效的荧光强度。所有混合物均含有 (S)-6和Zn(OAc)2(1:20)。
采用1H NMR研究了探针(S)-6对色氨酸的手性识别机制。(S)-6、(S)-6 + Zn(OAc)2、(S)-6 + Zn(OAc)2与L-Trp、(S)-6 + Zn(OAc)2与D-Trp的4个样品的1H NMR结果表明,(S)-6给出了两个单重态,一个是醛基团的醛基质子的d 10.17,另一个是萘基质子邻位的d 8.63。当添加Zn(OAc)2时,这两个单重态没有明显变化,而添加L-Trp或D-Trp时, d 10.17处单重态消失,可以推测醛基参与了与Trp的反应。图10为推导出的(S)-6和色氨酸对映体的分子结构并通过密度泛函理论(DFT)计算得到的相应的模型。由此作者认为,在水溶液中锌(II)存在的情况下,探针(S)-6用对映体氨基酸处理时,氨基酸的D-对映体和L-对映体形成的锌(II)配合物的结构和稳定性不同,会产生对映选择性荧光反应。
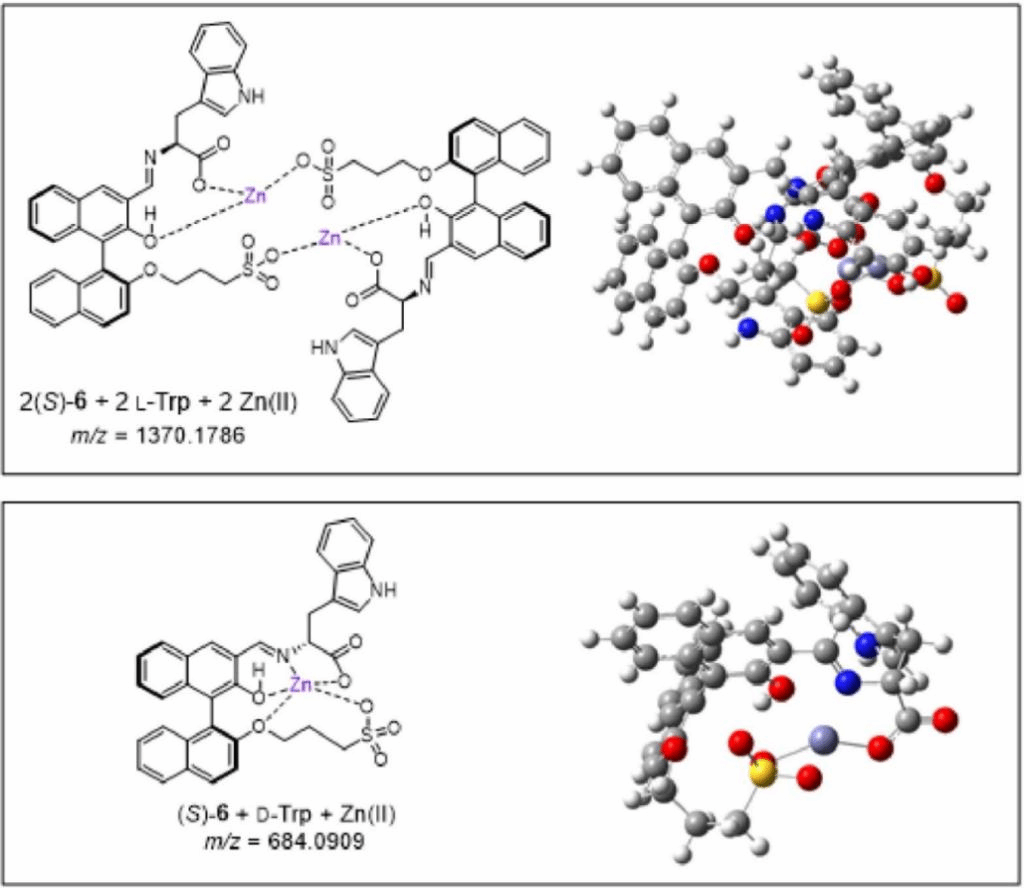
图10 在Zn(OAc)2的存在下,推导了(S)-6和色氨酸对映体混合物的结构并建立了模型。
综上所述,作者设计了一种水溶性的BINOL基荧光探针(S)-6,易于在温和的反应条件下通过简单的合成方法制备,这有利于其在水中氨基酸的对映选择性识别中应用。探针(S)-6在水溶液中微摩尔浓度下,对15种常见氨基酸表现出优异的对映选择性。 (S)-6对氨基酸的荧光响应在室温下放置30min后达到最大,并在随后的5.5 h内保持稳定。其及时性和优异的荧光稳定性使得(S)-6在手性荧光分析中具有很大的应用潜力。
文字 王诺
审核 叶曦翀
参考文献:DOI: 10.1016/j.cclet.2023.108345
https://doi.org/10.1016/j.cclet.2023.108345