手性化合物在药物,农药,兽药,香料中都广泛存在,同时也是先进手性材料的关键组成部分。高效分离对映体具有重大的科学意义和实用价值。而结晶拆分法因其简单、低成本,是目前大部分手性药物及其中间体最重要的生产方式[1]。但是传统的优先结晶法适用范围窄、单次结晶产率低。Lahav等人提出逆向结晶法[2],通过加入“量身定制”的聚合物抑制剂,抑制与之相同构型底物的成核生长,相反构型底物不受影响而较快析出。一定程度上提高了晶体光学纯度及产率。然而,传统的抑制剂都是通过单体聚合而来,其合成困难,官能团耐受度低,不利于结构筛选;且拆分的底物仍局限于簇集晶体和少量层状孪晶;对常用药物的拆分鲜有报道。阻碍了该方法的实际应用。
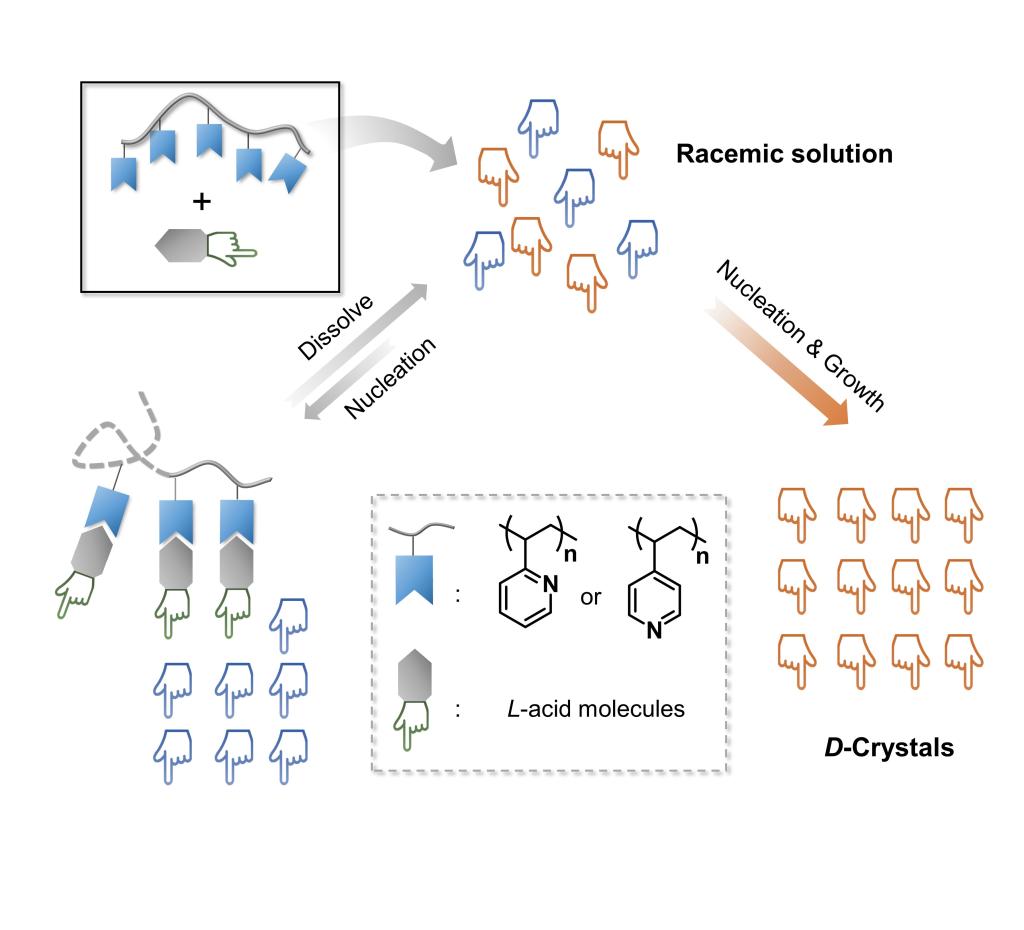
在本工作中,我们利用非共价相互作用,将手性小分子锚定在非手性聚合物主链上,制备了一系列超分子聚合物抑制剂。仅需改变客体小分子结构就能适用于不同底物的选择性结晶。极大简化了制备难度、降低了成本,并且分子结构更加多样化,便于快速的结构筛选。我们优先选择聚(4-乙烯基吡啶)(P4VP)作为主体,含有羧基或者磺酸基的手性小分子作为客体,通过离子键或者氢键进行复合。实验证明通过改换不同的小分子可以实现多种氨基酸及其衍生物的选择性结晶。值得一提的是,将小分子改为天冬氨酸时可以实现“外消旋晶体”——谷氨酸的选择性结晶。此外我们还实现了一种常用抗高血压药物——尼莫地平的直接拆分。另外,该策略不仅适用于水溶液体系,同样也适用于醇类,有机溶剂体系等。我们预期通过合理使用各种非共价相互作用,更多的聚合物添加剂可以被如法炮制,例如近年来被广泛研究的用于手性拆分的微/钠粒子,有机/无机杂化颗粒等。这将大大促进添加剂辅助的高效立体选择性结晶策略的发展。
关键词:手性药物;分级结晶;非共价相互作用;手性拆分;聚合物抑制剂
参考文献
[1] H. Lorenz, A. Seidel-Morgenstern, Angew. Chem. Int. Ed. 2014, 53, 1218-1250.
[2] D. Zbaida, L. Leiserowitz, M. Lahav, et. al., React. Polym. 1987, 6: 241-253.